Категории
Сменить пароль!
Сброс пароля!


Целью данного рандомизированного исследования IIIb фазы была оценка величины и стойкости клинического эффекта трехкомпонентной терапии у пациентов в возрасте 12 лет и старше с муковисцидозом и наличием гомозиготности по мутации F508del в гене CFTR.
У пациентов с муковисцидозом трехкомпонентная терапия (элексакафтор, тезакафтор и ивакафтор) безопасна, хорошо переносится и обеспечивает большую эффективность по сравнению с комбинированной терапией тезакафтором и ивакафтором.
Целью данного рандомизированного исследования IIIb фазы была оценка величины и стойкости клинического эффекта трехкомпонентной терапии у пациентов в возрасте 12 лет и старше с муковисцидозом и наличием гомозиготности по мутации F508del в гене CFTR.
В это двойное слепое многоцентровое исследование с контролем по активному препарату включили 176 участников со стабильным заболеванием и объемом форсированного выдоха (ОФВ1) 40–90 %. После 4-недельного вводного периода, в течение которого участники получали тезакафтор внутрь в дозе 100 мг один раз в сутки (1 р/сут) и ивакафтор в дозе 150 мг каждые 12 часов, 175 участников были рандомизированы в соотношении 1 : 1 для получения лечения в течение 24 недель в составе следующих групп: 1) элексафтор внутрь в дозе 200 мг 1 р/сут + тезакафтор внутрь в дозе 100 мг 1 р/сут + ивакафтор внутрь в дозе 150 мг каждые 12 часов (элексакафтор + тезакафтор + ивакафтор, группа 1, n = 87)); или 2) тезакафтор внутрь в дозе 100 мг 1 р/сут + ивакафтор внутрь в дозе 150 мг каждые 12 часов (тезакафтор + ивакафтор, группа 2, n = 88).
Во время скринингового визита для проведения рандомизации учитывали прогнозируемый ОФВ1 в процентах, возраст и то, получал ли пациент модуляторы регулятора трансмембранной проводимости при муковисцидозе (CFTR).
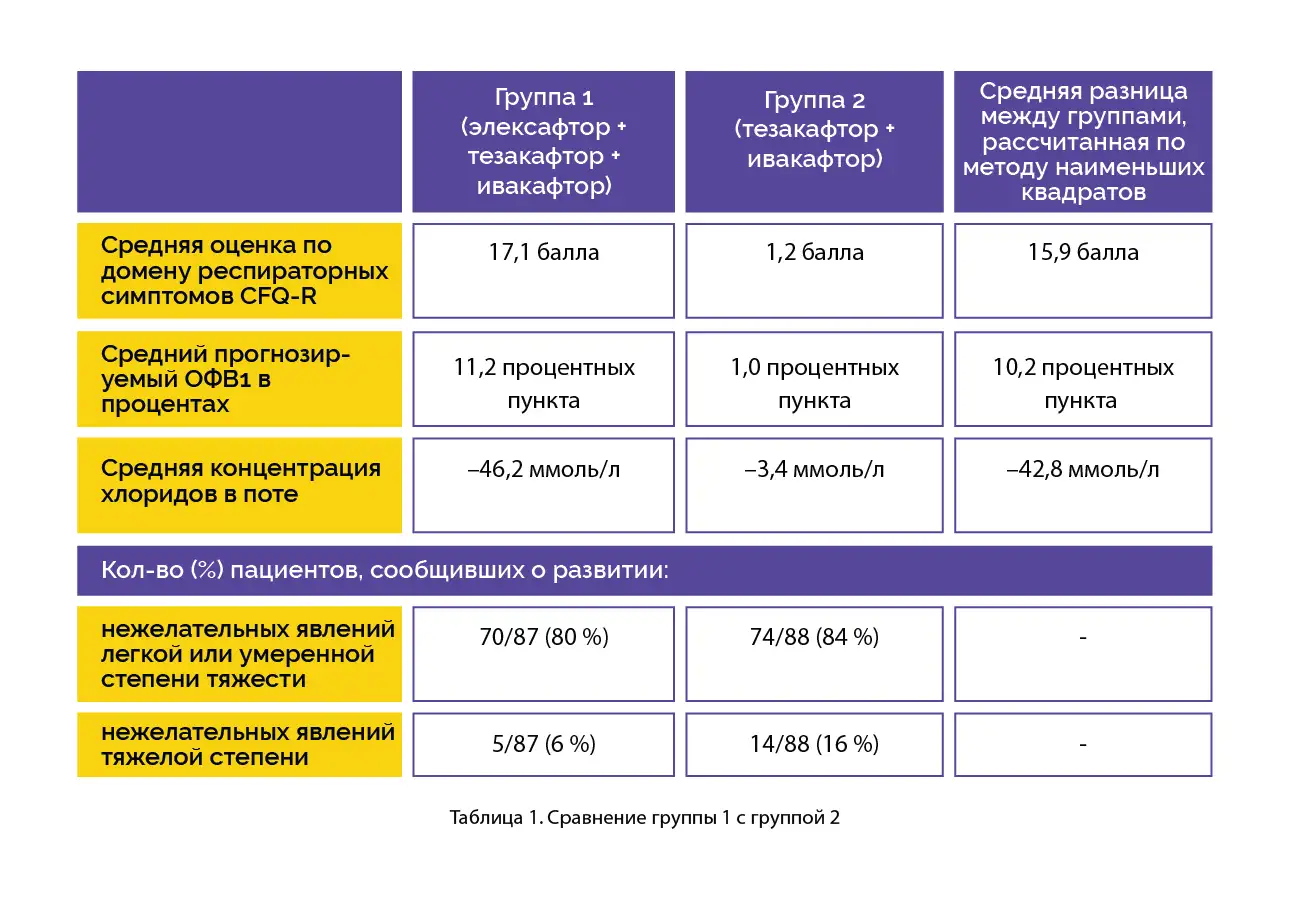
Основной конечной точкой было абсолютное изменение оценки по домену респираторных симптомов пересмотренного опросника для оценки качества жизни при муковисцидозе (CFQ-R) через 24 недели относительно исходного уровня. Дополнительной конечной точкой было абсолютное изменение прогнозируемого ОФВ1 в процентах через 24 недели относительно исходного уровня. Дополнительными конечными точками также были переносимость, безопасность и абсолютное изменение концентрации хлоридов в поте через 24 недели относительно исходного уровня.
По сравнению с исходным уровнем через 24 недели в обеих группах наблюдалось увеличение средней оценки по CFQ-R и среднего прогнозируемого ОФВ1 в процентах. При этом в обеих группах также наблюдалось уменьшение средней концентрации хлоридов в поте. Большинство участников сообщили о развитии нежелательных явлений легкой или умеренной степени тяжести. Также сообщалось о развитии нежелательных явлений тяжелой степени (см. таблицу 1).
Следует отметить, что 1 участник из группы 1 досрочно прекратил лечение по причине развития нежелательного явления (депрессия и тревога). При этом в группе 2 досрочно прекратили лечение 2 участника (у 1 пациента возникло психотическое расстройство, и еще у 1 пациента — обсессивно-компульсивное расстройство).
Можно сделать вывод о том, что трехкомпонентная терапия хорошо переносилась и была безопасной у пациентов с муковисцидозом. Кроме того, она обеспечила улучшение функций белка CFTR, качества жизни, связанного с состоянием дыхательной системы, и функции легких. Изменения были стойкими в течение 24 недель и более выраженными, чем при проведении комбинированной терапии тезакафтором и ивакафтором.
The Lancet Respiratory Medicine
Efficacy and safety of elexacaftor plus tezacaftor plus ivacaftor versus tezacaftor plus ivacaftor in people with cystic fibrosis homozygous for F508del-CFTR: a 24-week, multicentre, randomised, double-blind, active-controlled, phase 3b trial
Sivagurunathan Sutharsan и соавт.
Комментарии (0)