Категории
Сменить пароль!
Сброс пароля!


Инъекции цефтобипрола медокарила натрия эффективны при 3 острых бактериальных инфекциях.
В пресс-релизе от апреля 2024 года Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) одобрило инъекционную терапию цефтобипрола медокарилом у взрослых бактериемии, вызванной Staphylococcus aureus (SAB), инфекционного эндокардита нативных клапанов правых отделов сердца, острых инфекций кожи и подкожной клетчатки (SSSI). Также данный антибиотик одобрен для лечения внебольничной пневмонии (ВП) у детей (в возрасте от 3 месяцев до 18 лет) и взрослых.
Одобрение новых показаний к применению основано на результатах исследований по оценке эффективности инъекций цефтобипрола медокарила натрия при различных бактериальных инфекциях:
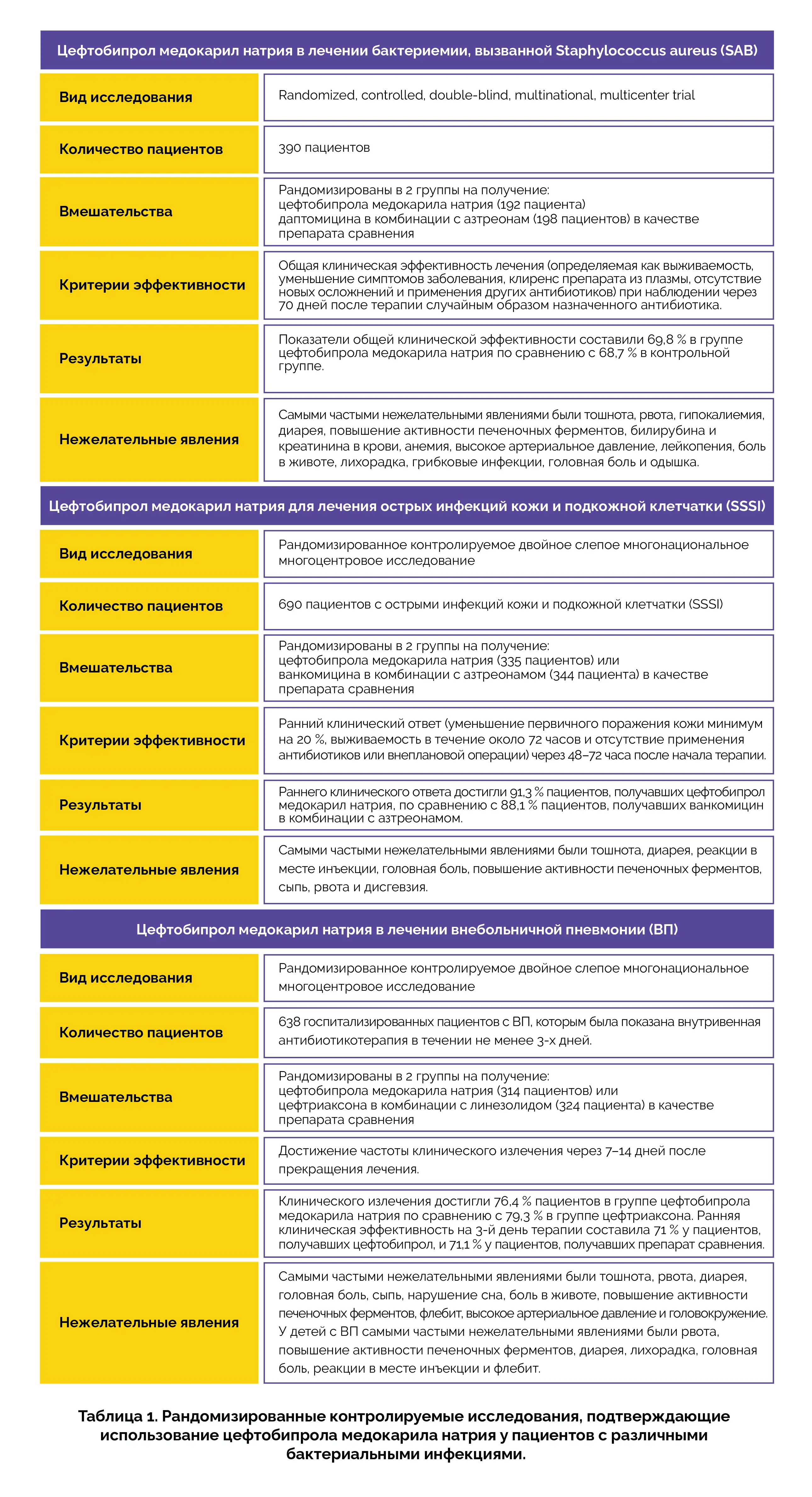
Перед началом применения цефтобипрола медокарила натрия необходимо учесть следующее:
Цефтобипрол медокарил натрия противопоказан пациентам с тяжелыми реакциями гиперчувствительности к препарату в анамнезе (документально подтвержденными), повышенной чувствительностью к компонентам препарата или другим цефалоспоринам.
В инструкции к препарату цефтобипрол имеются предостережения и рекомендации о повышении риска смерти у пациентов с ИВЛ-ассоциированной бактериальной пневмонией (использование препарата по незарегистрированным показаниям), а также о повышении риска реакций гиперчувствительности, судорог, других изменений со стороны центральной нервной системы, инфекционной диареи, вызванной Clostridioides difficile.
FDA News Release
https://www.fda.gov/news-events/press-announcements/fda-approves-new-antibiotic-three-different-uses
FDA Approves New Antibiotic for Three Different Uses
Комментарии (0)