Категории
Сменить пароль!
Сброс пароля!


В исследовании применения селаделпара были получены перспективные результаты относительно лечения первичного билиарного холангита, ранее известного как первичный билиарный цирроз печени.
Данные нового клинического исследования, в котором приняли участие пациенты с первичным билиарным холангитом, свидетельствуют о более выраженном биохимическом ответе и нормализации активности щелочной фосфатазы при применении селаделпара по сравнению с плацебо. Кроме того, при применении селаделпара (агониста дельта-рецепторов, активируемых пероксисомными пролифераторами (PPARδ)) было отмечено снижение интенсивности зуда среднетяжелой степени.
В общей сложности 193 пациента (с неудовлетворительным ответом на применение урсодиола или развитием побочных эффектов на применение этого препарата в анамнезе) были рандомизированы (в соотношении 2 : 1) в группу лечения селаделпаром в дозе 10 мг внутрь ежедневно или в группу плацебо.
Основной конечной точкой исследования было достижение биохимического ответа через один год после начала лечения. Дополнительными конечными точками были нормализация активности щелочной фосфатазы (ЩФ) через один год после начала лечения и оценка различий по показателю интенсивности зуда через 6 месяцев после начала лечения у пациентов с зудом среднетяжелой степени на момент начала исследования.
Из общего числа пациентов 93,8 % получали урсодиол в качестве стандартной фоновой терапии. Достижение биохимического ответа в группе применения селаделпара было отмечено у большего числа пациентов по сравнению с группой плацебо. Кроме того, в группе применения селаделпара чаще наблюдалась нормализация активности ЩФ (p < 0,001; см. таблицу 1).
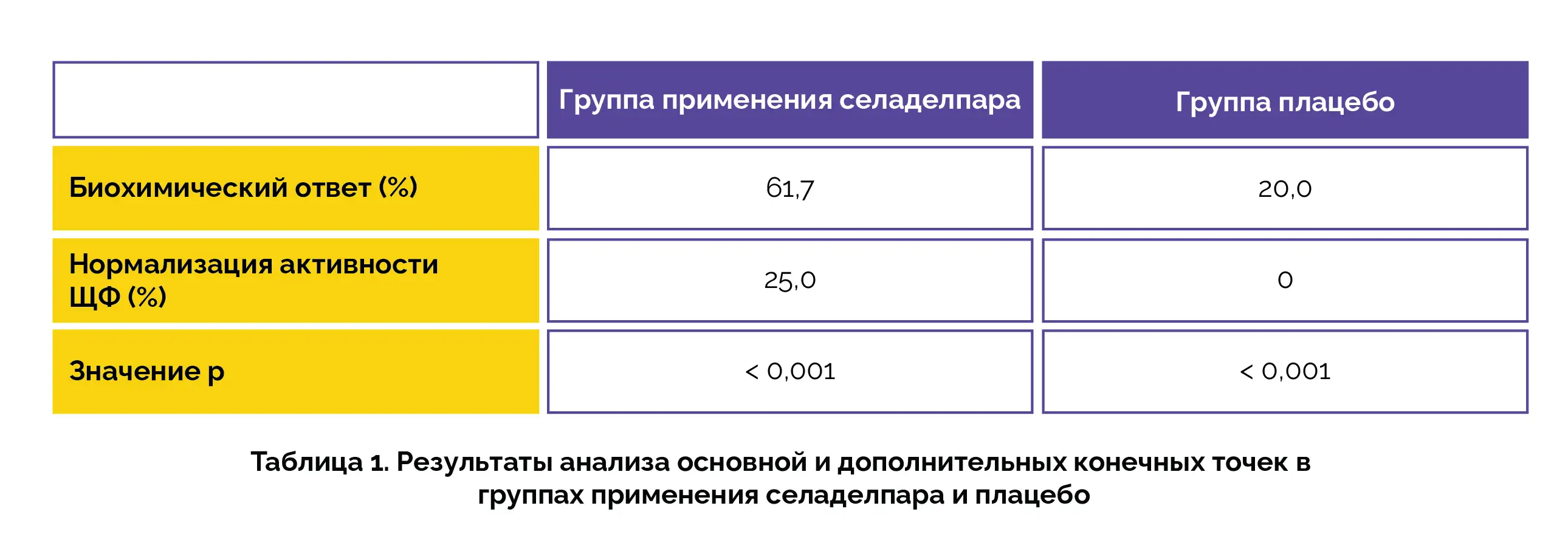
Кроме этого, при применении селаделпара более выраженным было снижение интенсивности зуда по сравнению с группой плацебо. Развитие нежелательных явлений было зарегистрировано у 86,7 % и 84,6 % пациентов в группе применения селаделпара и плацебо, а серьезных нежелательных явлений — у 7 % и 6,2 % пациентов соответственно.
The New England Journal of Medicine
A Phase 3 Trial of Seladelpar in Primary Biliary Cholangitis
Gideon M Hirschfield и соавт.
Комментарии (0)