Категории
Сменить пароль!
Сброс пароля!


Ублитуксимаб, моноклональное антитело с низким содержанием фукозы, нацеленное на специфический эпитоп поверхностного антигена CD20, применяют в лечении рецидивирующих форм рассеянного склероза.
Ублитуксимаб, моноклональное антитело с низким содержанием фукозы, нацеленное на специфический эпитоп поверхностного антигена CD20, применяют в лечении рецидивирующих форм рассеянного склероза [1,2]. Эта крупная белковая молекула с молекулярной массой 147 000 Да является первым и единственным моноклональным антителом, направленным на антиген CD20, которое применяют в лечении этого заболевания [2,3]. В декабре 2022 г. Управление по контролю качества продуктов питания и лекарственных средств США (FDA) одобрило применение этого препарата у пациентов с рецидивирующими формами рассеянного склероза по схеме одна часовая инфузия два раза в год после введения начальной дозы препарата.
Фармакологическая группа: моноклональные антитела к CD20 [2]
У взрослых применение ублитуксимаба, антитела, полученного с применением технологий гликоинжиниринга, показано в лечении рецидивирующих форм рассеянного склероза (РС), таких как
Патогенез некоторых видов рака и аутоиммунных заболеваний, таких как заболевание, ассоциированное с антителами класса IgG к миелин-олигодендроцитарному гликопротеину, расстройства спектра оптиконейромиелита и рассеянный склероз, связан с нарушением регуляции В-клеток. Антиген CD20 экспрессируют часть CD3-положительных Т-клеток, пре‑В‑клетки, В-клетки памяти и зрелые/незрелые В-клетки. Таким образом, антитела к CD20 могут вызывать фагоцитоз, опосредованный Fc-гамма-рецепторами (FcγR) (антителозависимую клеточную цитотоксичность (АЗКЦ)), активацию путей системы комплемента и истощение В‑клеток путем их прямого уничтожения. Несмотря на разработку различных антител к CD20, лечению с их применением препятствовала низкая экспрессия CD20 злокачественными клетками при таких заболеваниях, как В-клеточный хронический лимфолейкоз, и субоптимальная интенсивность антителозависимой цитотоксичности.
В отличие от других одобренных к применению антител, включая окрелизумаб, обинутузумаб, офатумумаб и ритуксимаб, ублитуксимаб связывается с эпитопом CD20 с константой связывания, сравнимой с ритуксимабом. Для улучшения взаимодействия ублитуксимаба с FcγR, в частности с FcγRIIIA (CD16), экспрессируемыми макрофагами и естественными клетками-киллерами, этот препарат получают на линии клеток YB2/0 крыс с низкой концентрацией фукозы (24 % по сравнению с 93 % при производстве ритуксимаба).
Благодаря этому при применении ублитуксимаба усиливается АЗКЦ, в том числе в отношении злокачественных клеток с минимальной экспрессией CD20. Точный механизм действия ублитуксимаба при его применении в лечении рассеянного склероза неясен, однако предполагается, что препарат приводит к связыванию CD20 и последующему лизису клеток [2].
a) 150 мг в виде внутривенной инфузии в качестве начальной дозы,
b) 450 мг в качестве второй внутривенной инфузии через 2 недели после введения начальной дозы,
c) 450 мг в виде внутривенной инфузии через 24 недели после введения начальной дозы, а затем каждые 24 недели в качестве последующих инфузий.
Всасывание
В день после введения ублитуксимаба в одобренной рекомендуемой дозе средняя Cmax составляла 139 мкг/мл, а средняя геометрическая площадь под фармакокинетической кривой в равновесном состоянии (AUC) — 3000 мкг/мл. У лиц с рецидивирующим рассеянным склерозом экспозиция препарата при его введении в диапазоне доз от 150 до 600 мг увеличивалась пропорционально дозе.
Объем распределения
Оценочный центральный объем распределения ублитуксимаба составляет 3,18 л.
Связывание с белками
Данные отсутствуют.
Метаболизм
В метаболизме ублитуксимаба, по всей видимости, принимают участие неспецифические протеолитические ферменты, которые разрушают его до более мелких пептидов и аминокислот.
Выведение
Данные отсутствуют.
Период полувыведения
Оценочный средний конечный период полувыведения ублитуксимаба составляет 22 дня.
Клиренс
Данные отсутствуют [2].
Применение ублитуксимаба противопоказано при наличии:
При одновременном применении ублитуксимаба с другими иммунодепрессантами и иммуномодулирующими препаратами, такими как кортикостероиды в подавляющих иммунную систему дозах, может повышаться риск развития инфекций. При одновременном применении ублитуксимаба с иммунодепрессантами необходимо учитывать возможность их аддитивного воздействия на иммунную систему.
При переходе с лекарственных препаратов, воздействующих на иммунную систему, необходимо учитывать механизм действия и продолжительность применения этих препаратов ввиду возможного аддитивного иммуносупрессивного эффекта при начале лечения ублитуксимабом[5].
Серьезные побочные эффекты при применении ублитуксимаба включают:
a) Снижение концентрации иммуноглобулинов
Ублитуксимаб может приводить к снижению концентрации некоторых типов антител.
b) Инфекции
c) Инфузионные реакции
Безопасность, эффективность и переносимость ублитуксимаба при его применении в лечении рецидивирующих форм рассеянного склероза
В плацебо-контролируемом исследовании II фазы, проведенном Fox E и соавт., введение ублитуксимаба в виде инфузии было безопасным, хорошо переносилось и обеспечивало выраженное истощение В-клеток, а также статистически значимое снижение частоты рецидива и активности заболевания по данным магнитно-резонансной томографии (МРТ). Участников исследования разделили на 6 дозировочных групп, которые получали по три инфузии ублитуксимаба (150 мг в течение 1–4 часов в 1-й день и по 450–600 мг в течение 1–3 часов на 15‑й день и через 24 недели). Основной установленной конечной точкой было истощение В‑клеток.
К 4-й неделе медиана показателя истощения В-клеток во всех группах (n = 48) составляла > 99 % и оставалась стабильной к 24-й и 48-й неделе. На 24-й и 48-й неделях накапливающие гадолиний очаги в режиме T1 отсутствовали, а объем очагов в режиме Т2 уменьшился на 10,6 %. Годовая частота рецидива в исследовании составила 0,07, при этом у 93 % участников рецидив отсутствовал (см. рисунок 1).
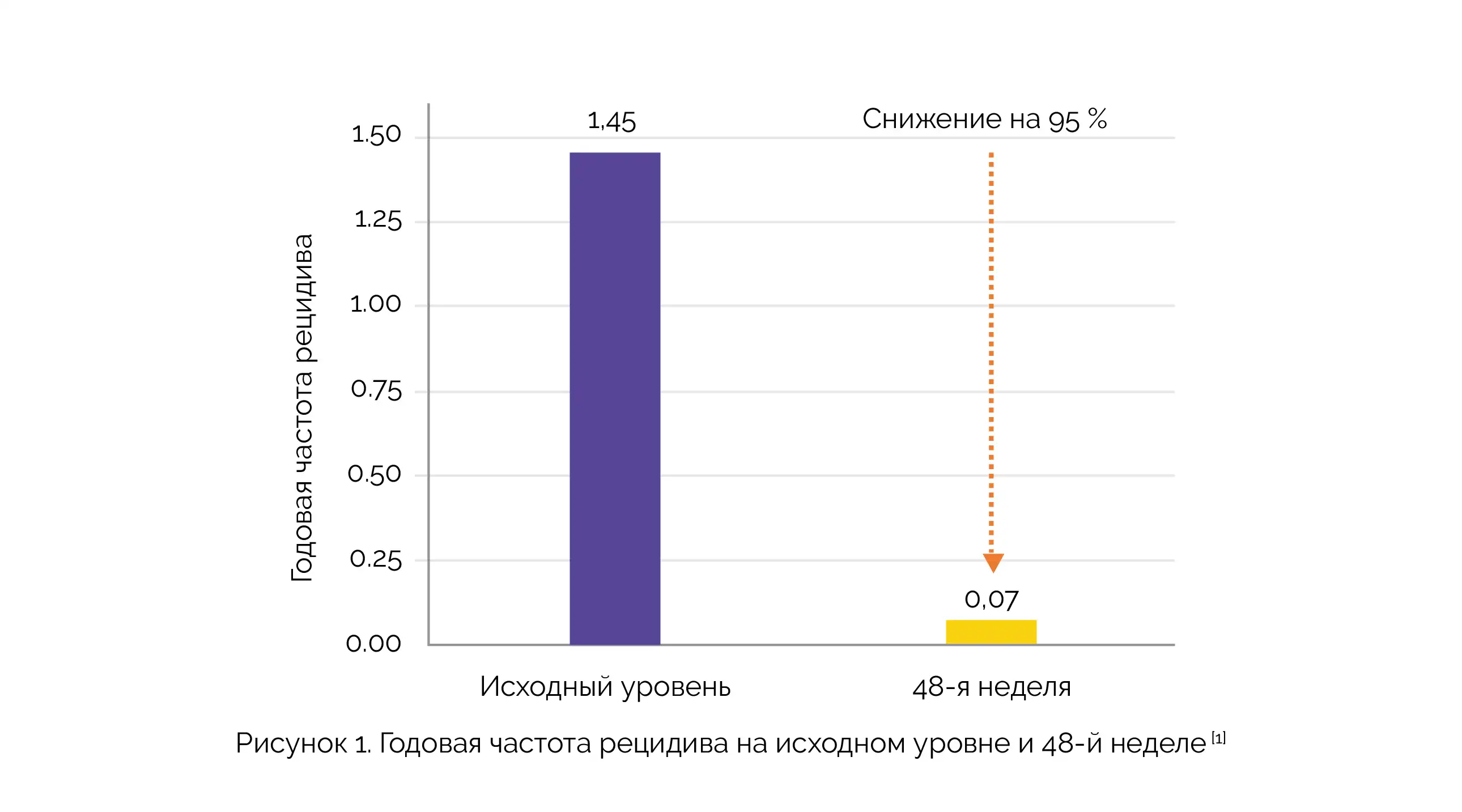
В этом исследовании у 74 % участников признаки активности заболевания отсутствовали. Большинство нежелательных явлений были инфузионными реакциями (все 1–2-й степени тяжести), без явного увеличения частоты их возникновения при инфузиях более короткой продолжительности. Случаев прекращения лечения по причине развития нежелательных явлений не было.
В анализе данных исследований ULTIMATE I и II, проведенном Cree B и соавт., установлено, что, помимо снижения выраженности нарушения жизнедеятельности по результатам запланированного анализа через 12 и 24 недели, в апостериорном анализе стойкости эффекта за 12 недель наблюдается снижение инвалидизации и улучшение оценок в тесте установки девяти колышков в лунки и тесте оценки времени прохождения 8 метров (25 футов), что является дополнительным свидетельством статистически значимого снижения нарушения жизнедеятельности при применении ублитуксимаба[6].
Применение ублитуксимаба по сравнению с терифлуномидом в лечении рассеянного склероза
В исследовании, проведенном Steinman L и соавт., участников с рецидивирующим рассеянным склерозом рандомизировали в группу внутривенного введения ублитуксимаба (в дозе 150 мг в 1‑й день, а затем в дозе 450 мг на 15-й день и через 24, 48 и 72 недели) и приема плацебо внутрь или в группу приема терифлуномида внутрь (в дозе 14 мг 1 р/сут) и внутривенного введения плацебо.
Основной конечной точкой была годовая частота рецидива, а дополнительными конечными точками — количество накапливающих гадолиний очагов на МРТ через 96 недель и усиление нарушения жизнедеятельности. В течение 96-недельного периода при применении ублитуксимаба у лиц с рецидивирующим рассеянным склерозом снизились годовая частота рецидива и количество очагов поражения в головном мозге на МРТ (но не риск усиления нарушения жизнедеятельности) по сравнению с применением терифлуномида [7].
С использованием компьютерной программы RevMan 5.4.1 был проведен метаанализ для оценки размера эффекта по таким показателям, как данные на МРТ, годовая частота рецидива, исходы по данным МРТ и признаки активности заболевания, через 2 года после начала лечения ублитуксимабом. В двух рандомизированных контролируемых исследованиях (N = 1094) было установлено, что размер эффекта (d Коэна) по показателю годовой частоты рецидива составляет –0,17 в пользу ублитуксимаба. По результатам анализа поражений на МРТ через 96 недель как в режиме T1 (d Коэна = –0,43), таки в режиме T2 (d Коэна = –0,55) ублитуксимаб превосходил терифлуномид по эффективности. У участников из группы применения ублитуксимаба активность заболевания была ниже (отношение шансов = 3,33) [8].
1. Fox E, Lovett-Racke AE, Gormley M, Liu Y, Petracca M, Cocozza S et al. A phase 2 multicenter study of Ublituximab, a novel glycoengineered anti-CD20 monoclonal antibody, in patients with relapsing forms of multiple sclerosis. Multiple Sclerosis Journal. 2021 Mar;27(3):420-9.
2. Ублитуксимаб. [На английском языке.] База данных Drug Bank. Инвентарный номер: DB11850. Доступно по ссылке: https://go.drugbank.com/drugs/DB11850 [Дата последнего доступа: 23 февраля 2023 г.]
3. База данных LactMed®. [В Интернет]. Издательство Bethesda (MD): Национальный институт охраны здоровья ребенка и развития человека; 2006 г. Ублитуксимаб. [Дата последнего обновления: 15 января 2023 г.]. Доступно по ссылке: https://www.ncbi.nlm.nih.gov/books/NBK588740/. Номер на книжной полке: NBK588740, PMID: 36701507
4. Faissner S, Gold R. Efficacy and Safety of Multiple Sclerosis Drugs Approved Since 2018 and Future Developments. CNS Drugs. 2022 Aug;36(8):803-817.
5. Ублитуксимаб. [На английском языке.] Инструкция по медицинскому применению, одобренная FDA. Доступно по ссылке: https://www.accessdata.fda.gov/drugsatfda_docs/label/2022/761238s000lbl.pdf [Дата последнего обращения: 23 февраля 2023 г.]
6. Cree B, Fox E, Hartung HP, Alvarez E, Qian P, Wray S et al. Disability Improvements With Ublituximab in Relapsing Multiple Sclerosis (RMS): Expanded Disability Status Scale (EDSS), 9-Hole Peg Test (9-HPT), and Timed 25-Foot Walk (T25FW) Evaluations From the Phase 3 ULTIMATE I and II Studies (P5-4.009). May 03, 2022; 98 (18 Supplement).
7. Steinman L, Fox E, Hartung HP, Alvarez E, Qian P, Wray S et al. Ublituximab versus Teriflunomide in Relapsing Multiple Sclerosis. The New England Journal of Medicine. 2022 Aug 25;387(8):704-714.
8. Mukhtar H, Yasmeen U, Siddiqa S, Sarfraz Z, Sarfraz A. Outcomes of Ublituximab compared to Teriflunomide for relapsing multiple sclerosis: A meta-analysis. Multiple Sclerosis and Related Disorders. 2022 Sep;65:104002.
Комментарии (1)