Категории
Сменить пароль!
Сброс пароля!


Тигециклин — это полусинтетический противомикробный препарат, который относится к классу глицилциклинов.
Тигециклин — это полусинтетический противомикробный препарат, который относится к классу глицилциклинов. Он был разработан для решения обостряющейся проблемы роста устойчивости бактерий к антибиотикам, включая Staphylococcus aureus. Препарат применяют в основном для лечения полимикробных инфекций, вызванных бактериями с множественной лекарственной устойчивостью [1,2].
17 июня 2005 г. Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) одобрило препарат в ускоренном режиме [2]. Тигециклин структурно похож на миноциклин. Молекулярные изменения позволили расширить спектр его действия и снизить вероятность развития резистентности к нему по сравнению с другими антибиотиками тетрациклинового ряда [3].
Фармакологический класс: антибиотики класса глицилциклинов [1]
Препарат применяют для лечения инфекций, вызванных чувствительными штаммами перечисленных микроорганизмов, при указанных ниже заболеваниях (таблица 1).

Тигециклин обладает широким спектром действия, которое основано на влиянии на синтез бактериального белка. Он связывается с субъединицей рибосомы 30S. Это действие блокирует проникновение молекул аминоацил-тРНК на А-сайт рибосомы. Это препятствует включению аминокислот в растущие пептидные цепи, останавливая выработку белка. В целом тигециклин относят к бактериостатическим препаратам, однако он проявлял бактерицидную активность против изолятов Streptococcus pneumoniae и Legionella pneumophila [3,4].
Доза тигециклина варьируется в зависимости от заболевания, для лечения которого его применяют. Ниже приведен краткий обзор рекомендуемых доз (таблица 2).
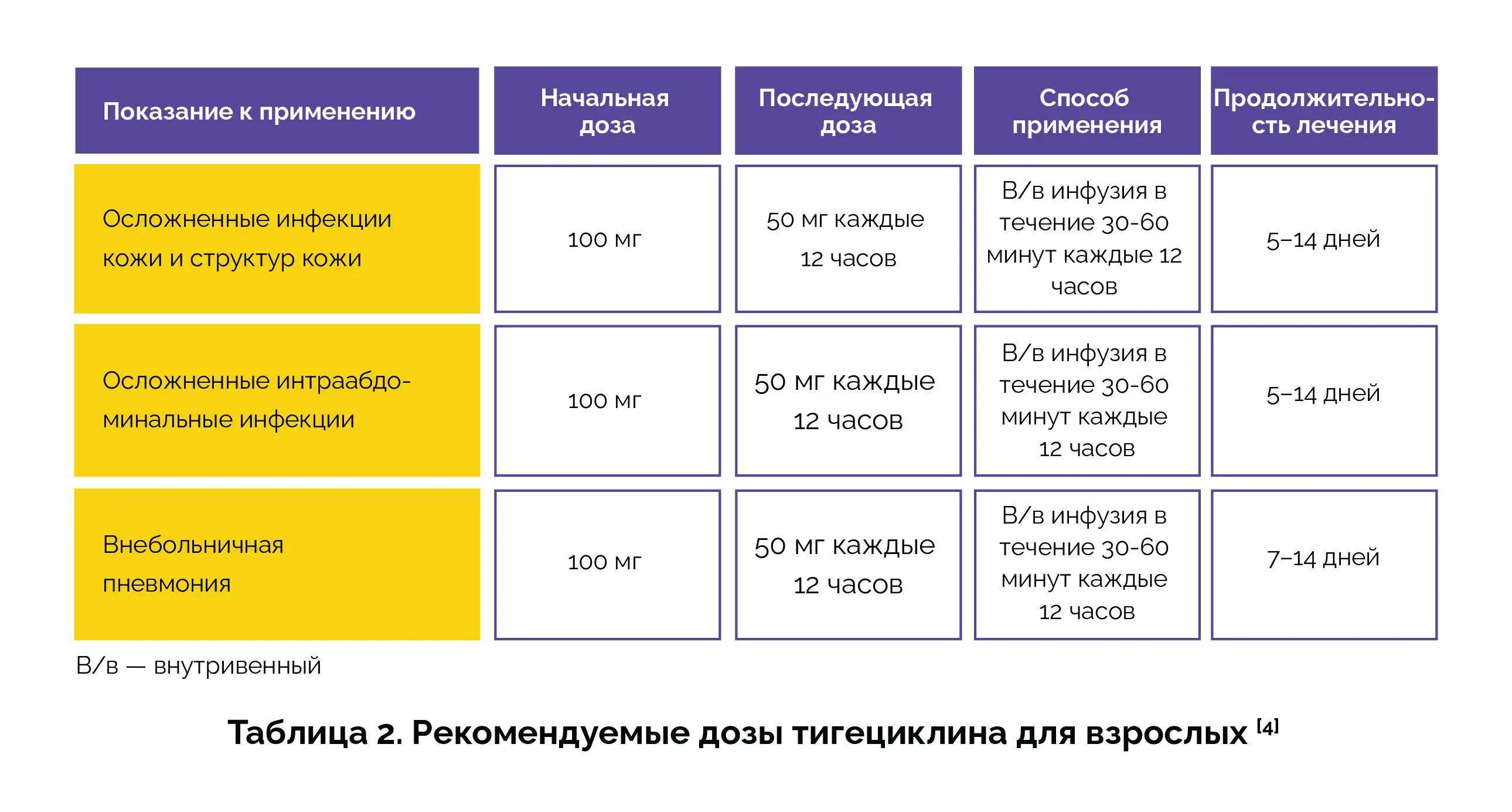
Продолжительность терапии должна зависеть от тяжести и локализации инфекции, а также от бактериологического и клинического ответа у пациента. В таблице 3 приведены дозы тигециклина для пациентов с почечной и печеночной недостаточностью.
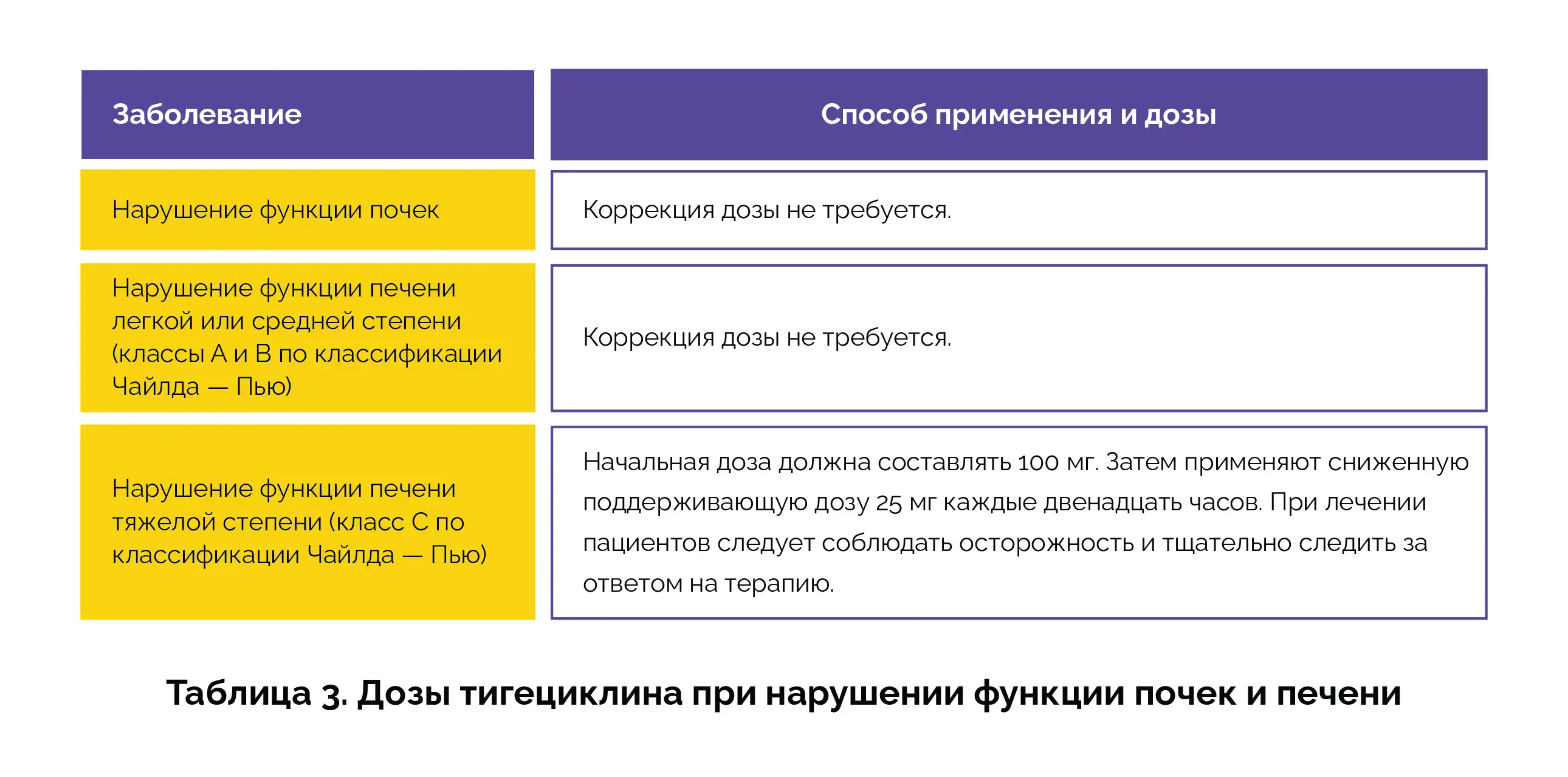
Дополнительное примечание. Тигециклин не следует применять у детей, за исключением случаев отсутствия альтернативных вариантов антибактериальной терапии [4,5].
В таблице 4 представлен подробный обзор фармакокинетического профиля тигециклина.
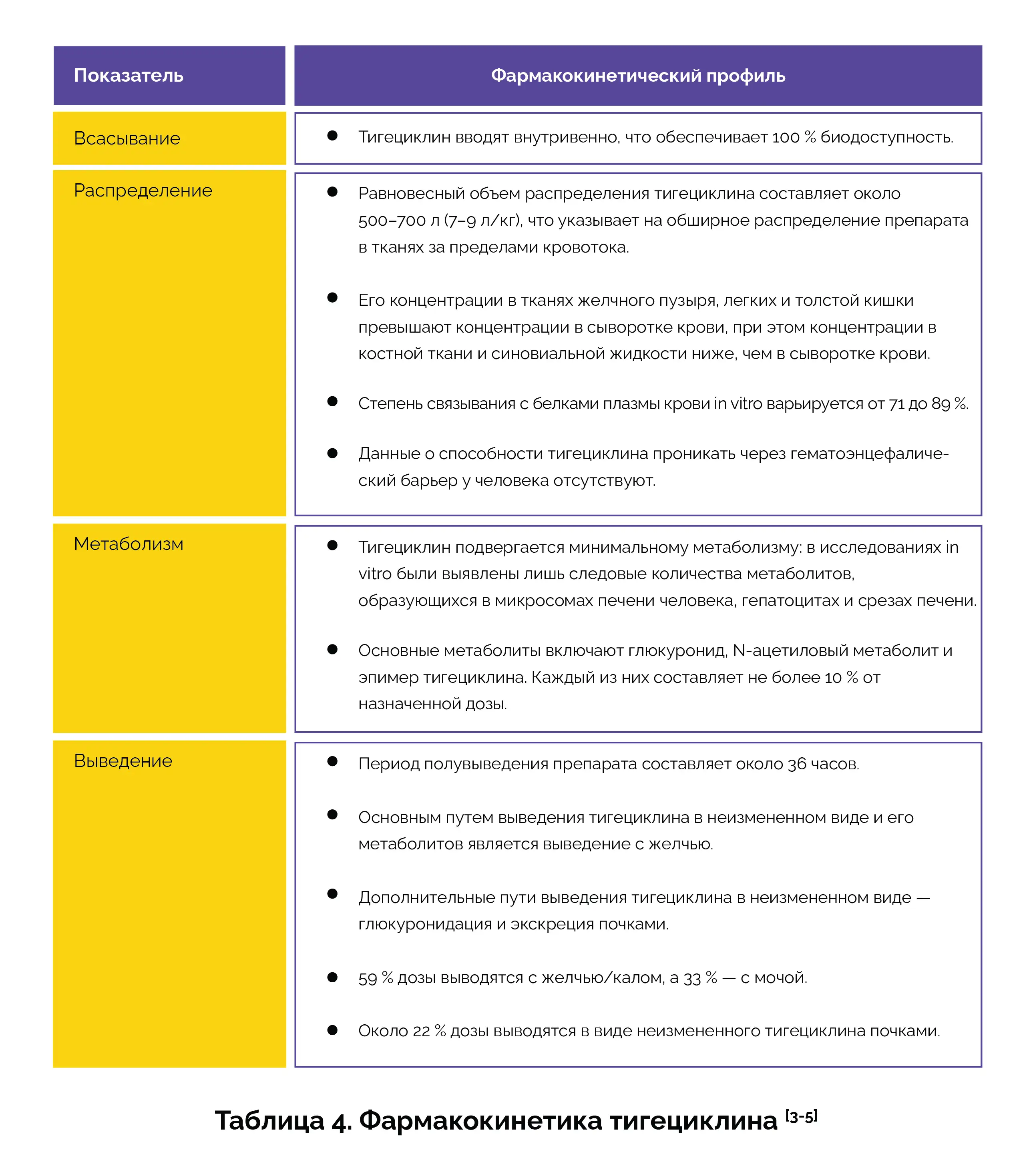
Инъекции тигециклина противопоказаны для лечения:
(a) синдрома диабетической стопы;
(b) внутрибольничной пневмонии или пневмонии, связанной с искусственной вентиляцией легких [4].
Примечание. В 2010 и 2013 гг. Управление по контролю качества пищевых продуктов и лекарственных средств США выпустило особое предупреждение о повышенном риске смерти при применении тигециклина, особенно у пациентов с пневмонией, связанной с искусственной вентиляцией легких [6].
(A) Варфарин. При применении тигециклина одновременно с варфарином следует контролировать протромбиновое время или выполнять другое исследование на угнетение свертывания крови.
(B) Оральные контрацептивы. Одновременное применение антибактериальных препаратов и оральных контрацептивов может снизить эффективность последних [4].
Наиболее частые побочные эффекты:
[1] Применение тигециклина при осложненных инфекциях кожи и мягких тканей
В исследовании, проведенном Montravers Р. и соавт., применение тигециклина как в качестве монотерапии, так и в составе комбинированной терапии обеспечивало благоприятные показатели клинического ответа у пациентов с осложненными инфекциями кожи и мягких тканей, характеризующимися тяжелым течением. Исследователи проанализировали данные 254 пациентов, получавших тигециклин для лечения инфекций в ходе 5 наблюдательных исследований, проведенных в Европе. У пациентов отмечалось тяжелое заболевание (средний показатель по шкале острых физиологических расстройств и хронических функциональных изменений [APACHE] II: 15,0, динамическая оценка органной недостаточности [SOFA]: 5,8), при этом 34,4 % из них находились в отделениях интенсивной терапии, а 54,5 % заразились инфекциями в больницах. Наиболее частыми участками локализации инфекции были конечности (62,4 %), при этом некротические инфекции наблюдались в 43,8 % случаев.
Частыми возбудителями были Staphylococcus aureus, Escherichia coli и Enterococcus faecium, при этом в 30,5 % случаев были выявлены устойчивые штаммы. Тигециклин применяли в качестве монотерапии (71,8 %) или в составе комбинированной терапии (28,2 %) в среднем в течение 12 дней. Частота клинического ответа составила в целом 79,6 %, 86,7 % при монотерапии, 75,0 % при нозокомиальных инфекциях и 75,3 % в отношении оценок по шкале APACHE II > 15. Эти результаты подтверждают эффективность тигециклина в борьбе с тяжелыми осложненными инфекциями кожи и мягких тканей в условиях клинической практики [7].
[2] Сравнение тигециклина и меропенема при лечении послеоперационных осложненных интраабдоминальных инфекций
В исследовании с участием 56 пациентов с послеоперационными осложненными интраабдоминальными инфекциями при опухолях брюшной полости сравнивали эффективность и безопасность применения тигециклина и меропенема. Пациенты были разделены на 2 группы: 30 пациентов получали меропенем, а 26 пациентов — тигециклин. Показатели клинической эффективности в конце терапии и при выписке составили 83,33 % и 76,67 % для меропенема по сравнению с 76,92 % и 88,46 % для тигециклина соответственно. В исследовании был сделан вывод о том, что тигециклин также эффективен и безопасен как меропенем при лечении послеоперационных осложненных внутрибрюшных инфекций у пациентов с опухолями брюшной полости, т. е. не уступает меропенему [8].
[3]. Применение тигециклина в высоких дозах (ТВД) при тяжелых инфекциях
Согласно результатам систематического обзора и метаанализа, включавшего 10 исследований с участием 593 пациентов, применение ТВД при лечении тяжелых инфекций приводило к более благоприятным исходам по сравнению с контрольной группой. Применение ТВД было связано с более низкой смертностью от любых причин (отношение шансов (ОШ) — 0,44), более высокой частотой клинического излечения (ОШ — 3,43) и более эффективной микробиологической эрадикацией (ОШ — 2,25) без повышения частоты развития побочных эффектов. Результаты анализа в подгруппах указывали на то, что применение ТВД было особенно полезно при лечении нозокомиальной пневмонии (ОШ — 0,39), инфекций кровотока (ОШ — 0,19) и смешанных инфекций (ОШ — 2,04), тогда как существенных различий при осложненных внутрибрюшинных инфекциях выявлено не было (ОШ — 2,04) [9]
[4]. Сравнение тигециклина и левофлоксацина при лечении внебольничной пневмонии
В рандомизированном исследовании III фазы сравнивали применение тигециклина и левофлоксацина у 418 госпитализированных пациентов с внебольничной пневмонией. Эти пациенты получали тигециклин или левофлоксацин внутривенно (в/в) с возможностью перехода на левофлоксацин для приема внутрь после введения не менее шести внутривенных доз. Длительность лечения составляла 7–14 дней. Частота излечения при оценке излеченности в группах была сопоставимой. В популяции, поддающейся клинической оценке, частота излечения составила 90,6 % при применении тигециклина и 87,2 % при применении левофлоксацина. В клинической модифицированной популяции для анализа, выполняемого исходя из допущения, что все пациенты получили назначенное лечение (c-mITT), частота излечения составила 78 % и 77,8 % соответственно.
Нежелательные явления немного различались: тошнота и рвота чаще наблюдались у пациентов, получавших тигециклин, тогда как повышенные уровни аланинаминотрансферазы и аспартатаминотрансферазы чаще наблюдались при применении левофлоксацина. Существенных различий в продолжительности госпитализации, длительности применения антибиотиков для внутривенного введения или приема внутрь, частоте повторной госпитализации или перехода на левофлоксацин для приема внутрь выявлено не было. В целом были подтверждены безопасность и эффективность (не меньшая эффективность) тигециклина по сравнению с левофлоксацином при лечении внебольничной пневмонии [10].
[5] Применение тигециклина для лечения инфекций мочевыводящих путей (ИМП), вызванных бактериями с множественной лекарственной устойчивостью
В рамках систематического обзора было изучено 27 случаев ИМП, вызванных бактериями с множественной лекарственной устойчивостью. К их числу относились 13 осложненных ИМП и 5 связанных с катетером ИМП, вызванных в основном бактериями Escherichia coli (n = 6), Acinetobacter baumannii (n = 9) и Klebsiella pneumonia (n = 11). Тигециклин применяли в виде монотерапии в 19 случаях и в сочетании с другими антибиотиками в 8 случаях, при этом медиана продолжительности лечения составила 13 дней.
Благоприятный клинический или микробиологический ответ наблюдался у 88,9 % пациентов (24/27), при этом у 4 пациентов симптомы возобновились в течение 3 месяцев. Было установлено, что тигециклин является потенциальным эффективным вариантом лечения ИМП, вызванных устойчивыми микроорганизмами, особенно в случаях неэффективности альтернативных противомикробных препаратов. Однако развитие рецидива у некоторых пациентов подчеркивает необходимость дальнейших исследований[11].
Комментарии (0)